Oncoimmunology. 2013 Aug 1; 2(8): e25769.
Lynda Thyer, Emma Ward, Rodney Smith, Jacopo JV Branca, Gabriele Morucci, Massimo Gulisano, David Noakes, Robert Eslinger, and Stefania Pacini
GC protein-derived macrophage-activating factor decreases α-N-acetylgalactosaminidase levels in advanced cancer patients
Фактор активации макрофагов, полученный из белка GC, снижает уровень α-N-ацетилгалактозаминидазы у больных раком на поздних стадиях.
α-N-ацетилгалактозаминидаза (нагалаза) накапливается в сыворотке крови онкологических больных и ее активность коррелирует с опухолевой нагрузкой, агрессивностью и клиническим течением заболевания.
Введение макрофагально-активирующего фактора GC-белка (GcMAF) онкологическим больным с повышенным уровнем нагалазы ассоциировалось со снижением активности нагалазы в сыворотке крови и со значительными клиническими преимуществами.
Здесь мы сообщаем о результатах введения GcMAF гетерогенной когорте пациентов с гистологически разнообразными, распространенными новообразованиями, которые обычно рассматриваются как «неизлечимые» заболевания. В большинстве случаев терапия GcMAF была начата на поздних стадиях прогрессирования опухоли.
Поскольку это открытый, неконтролируемый, ретроспективный анализ, следует проявлять осторожность при установлении причинно-следственных связей между введением GcMAF и исходом заболевания.
Тем не менее, реакция на GcMAF была в целом устойчивой, и наметились некоторые тенденции. У всех пациентов (n = 20) отмечалась повышенная активность нагалазы в сыворотке крови, значительно превышающая нормальные значения. У всех пациентов, кроме одного, наблюдалось достоверное снижение активности нагалазы в сыворотке крови при еженедельных инъекциях GcMAF. Снижение активности нагалазы ассоциировалось с улучшением клинических условий, и о неблагоприятных побочных эффектах не сообщалось. Представленные здесь наблюдения подтверждают и расширяют предыдущие результаты и прокладывают путь к дальнейшим исследованиям, направленным на оценку точной роли и показаний к противоопухолевой иммунотерапии на основе GcMAF.
Ключевые слова: рак, комплементарная медицина, иммунотерапия, макрофаги,
витамин D
Знакомство
Известно, что α-N-ацетилгалактозаминидаза (нагалаза) накапливается в сыворотке крови онкологических больных, где она опосредует дегликозилирование группоспецифического компонента (GC), наиболее известного как витамин D-связывающий белок (VDBP), который является предшественником макрофаг-активирующего фактора GC белка (GcMAF). Дегликозилированный VDBP не может быть преобразован в GcMAF1 и снижение уровня GcMAF, как сообщается, способствуют иммунодефициту у лиц с прогрессирующими новообразованиями.2
Повышение активности нагалазы, наблюдаемое у онкологических больных, в основном связано с тем, что злокачественные клетки выделяют ферментативно активную нагалазу.3 Таким образом, сывороточная активность нагалазы отражает не только опухолевую нагрузку и агрессивность, но и клиническое течение заболевания.4—7 В настоящее время оценка сывороточной активности нагалазы предлагается как достоверное средство определения клинической тяжести множественных новообразований.3
В сыворотке крови нагалаза действует как эндо- (но не как экзо-) фермент, будучи неспособной дегликозилировать N-ацетилгалактозамин (GalNAc) остаток GcMAF.5 Таким образом, циркулирующая нагалаза не может расщеплять экзогенный GcMAF.5—7 Это наблюдение позволило предположить, что пациенты с повышенной активностью нагалазы могут получить пользу от экзогенного введения GcMAF. Наряду с этим, было замечено, что GcMAF оказывает множественные противоопухолевые эффекты in vivo и in vitro, как в экспериментальных, так и в спонтанных моделях опухолей. Учитывая влияние GcMAF на макрофаги и их центральную роль в противоопухолевом иммунном ответе, GcMAF широко рассматривается как иммунотерапевтическое средство.7
Однако, помимо стимуляции опухолевых инфильтрирующих макрофагов,8 GcMAF не только непосредственно ингибирует пролиферацию различных раковых клеток человека in vitro,9,10 но и обращает вспять злокачественный фенотип клеток рака молочной железы человека.10 Кроме того, сообщается, что GcMAF ингибирует ангиогенез, тем самым лишая опухолевые поражения кислорода и питательных веществ, необходимых для прогрессирования опухоли и метастазирования.10—13
Недавно было высказано предположение, что противоопухолевые эффекты GcMAF опосредованы рецептором витамина D (VDR), и было продемонстрировано, что GcMAF стимулирует внутриклеточный сигнальный путь, воздействуя на циклический АМФ. Этот каскад сигнальной трансдукции на самом деле может быть ответственен за гибель злокачественных клеток, подвергшихся воздействию GcMAF.12 Взятые вместе, эти результаты in vitro и in vivo дают обоснование наблюдению о том, что GcMAF оказывают значительное противоопухолевое действие у пациентов с прогрессирующим раком (по крайней мере, у части их).5—7 Следует отметить, что в вышеупомянутых исследованиях противоопухолевые эффекты GcMAF оценивались путем измерения активности нагалазы сыворотки крови в качестве маркера опухолевой нагрузки и прогрессирования.2,3,14
Биологические эффекты GcMAF были задокументированы в различных экспериментальных системах и стали предметом более 50 рецензируемых статей, опубликованных за последние 20 лет.15 Из-за убедительного научного обоснования, лежащего в основе гуманного использования GcMAF у пациентов с прогрессирующим раком, сотни врачей во всех частях мира приняли этот подход для различных показаний, при которых он может оказаться полезным.
В данной статье мы представляем ряд клинических случаев, иллюстрирующих результаты, полученные при применении GcMAF пациентам с различными типами рака на поздних стадиях, с особым акцентом на влияние GcMAF на активность нагалазы в сыворотке крови. Мы прекрасно понимаем, что эти случаи, в силу их неоднородности и меньшего числа, можно считать анекдотическими.
Тем не менее, недавнее исследование, посвященное оценке клинической практики, настоятельно рекомендует проводить повторную оценку отдельных случаев, подобных представленным здесь.16
Таким образом, в то время как некоторые исследования представляют большую и впечатляющую статистику, полученную из больших клинических когорт, другие могут сообщать об ограниченном количестве заслуживающих внимания случаев, как это делаем мы здесь.
Согласно этому новому, авторитетному, эпистемологическому подходу, «все эти истории становятся доказательством того, что работает в медицине».16 Таким образом, мы считаем, что клинические случаи, описанные ниже, указывают на благотворное влияние применения GcMAF у пациентов с прогрессирующим раком, что побуждает к дальнейшим исследованиям, чтобы официально рассмотреть эту возможность.
Результаты
Средняя активность нагалазы в сыворотке крови, зарегистрированная в нашей когорте пациентов, составила 2,84 ± 0,26 нМ/мин/мг с диапазоном 1,00–5,60 нМ/мин/мг (Таблица 1). На момент повторного тестирования (средний интервал = 112 дней) средняя сывороточная активность нагалазы в процессе лечения GcMAF составляла 2,01 ± 0,22 нМ/мин/мг с диапазоном 1,00–3,20 нМоль/мин/мг. Разница между этими значениями была статистически значимой (р < 0,05).
Следует отметить, что ни один пациент из этой когорты первоначально не находился в пределах лабораторного референсного диапазона активности нагалазы в сыворотке крови (0,90–0,92 нМ/мин/мг). На момент заключительного тестирования (средний интервал = 263 дня) средняя сывороточная активность нагалазы в когорте пациентов составляла 1,59 ± 0,17 нМоль/мин/мг с диапазоном 0,60–2,80 нМ/мин/мг. Разница между этим значением и сывороточной активностью нагалазы, зарегистрированной до начала лечения GcMAF, также была статистически значимой (p < 0,01).
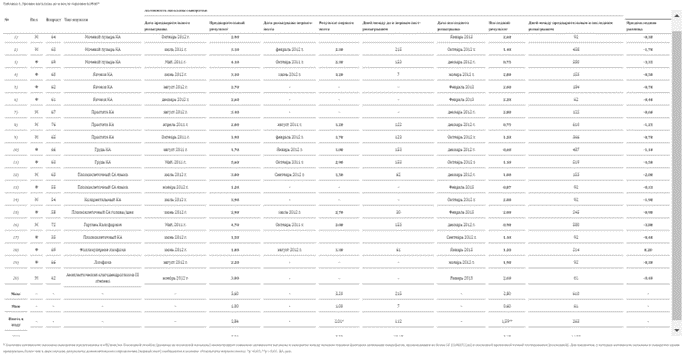
* Значения активности нагалазы в сыворотке крови представлены в виде нМ/мин/мг. В последнем столбце (разница между нагалазой и нагалазой до последнего) показано снижение активности нагалазы в сыворотке крови в период между началом терапии макрофаг-активирующим фактором (GcMAF), полученной из белка ГК, и последней точкой тестирования (последней). Для пациентов, у которых активность нагалазы в сыворотке крови была проверена более чем в двух случаях, результаты дополнительного определения (первого поста) сообщаются в графе «Результаты первого поста». *p < 0,05; **p < 0,01. СА, карцинома.
Описательное описание некоторых известных клинических случаев из Нидерландов
Следующие отчеты были собраны и переданы д-ром Стивеном Хофманом (CMC, Capelle aan den Ijssel; Нидерланды) и относятся к 2011–2012 годам. В дополнение к GcMAF большинству пациентов были назначены добавки витаминов D и A.
Дополнительные добавки показаны при их приеме. Большинство пациентов не принимали традиционную противоопухолевую химиотерапию вместе с GcMAF.
Тем не менее, несколько пациентов были подвергнуты традиционной противоопухолевой терапии в предыдущие годы, как указано в отдельных отчетах. Когда пациенты принимали традиционные терапевтические средства, такие как гормоны, в ходе введения GcMAF (например, пациент #8), это указывается в индивидуальном отчете.
При отсутствии иных показаний пациенты получали 100 нг GcMAF еженедельно в виде однократной внутримышечной инъекции в соответствии с общепринятыми рекомендациями.5—7 Оригиналы отчетов выделены курсивом. Каждый случай обозначается прогрессивными числами, как в Таблица 1.
В Рисунок 1, снижение активности нагалазы в сыворотке крови в когорте пациентов построено в зависимости от последовательного тестирования. Следует отметить, что, поскольку это ретроспективный анализ, а не клиническое исследование, определение нагалазы не проводилось в один и тот же момент времени у каждого отдельного пациента. Общая форма графика, однако, очень похожа, если не полностью накладывается на форму других графов того же типа, о которых сообщалось ранее.5—7,17
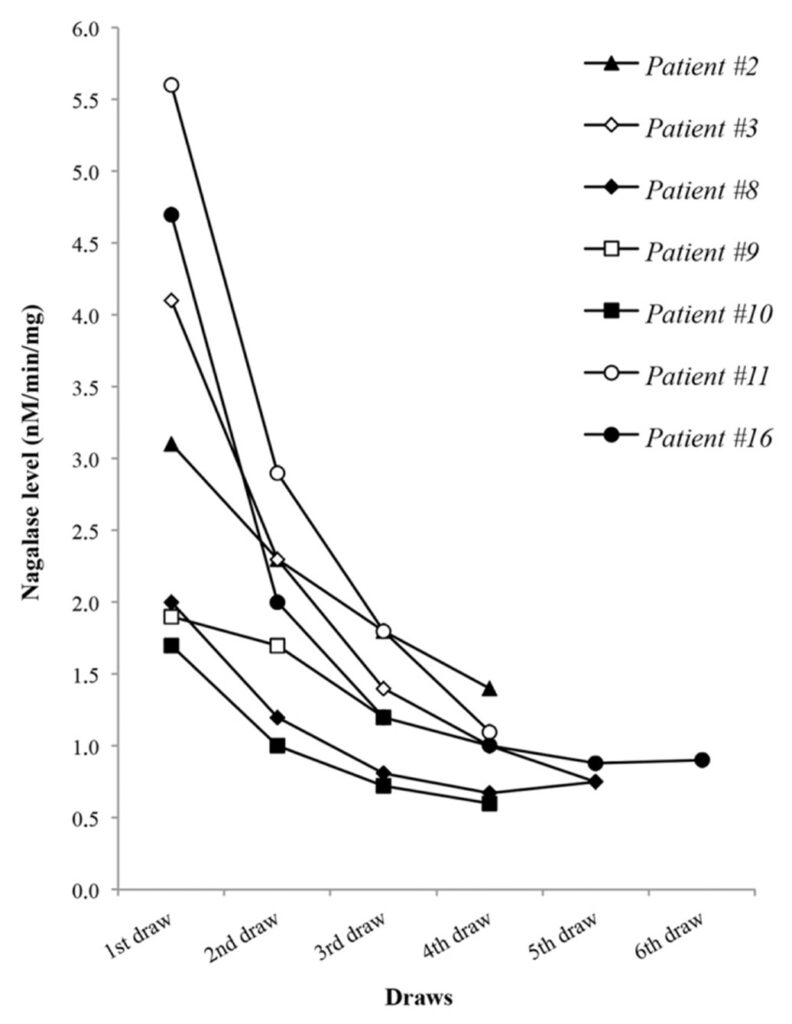
Рисунок 1. Временной курс лечения GcMAF у 7 онкологических больных с прогностическим показателем сывороточной активности нагалазы. Данные соответствуют пациентам, описанным в разделе «Описательное описание некоторых примечательных клинических случаев из Нидерландов». Определение активности нагалазы в сыворотке крови не проводилось в один и тот же момент времени у каждого отдельного пациента, как подробно описано в Таблица 1. Пациенты обозначаются порядковыми номерами, как в разделе «Результаты» и Таблица 1.
- Мужчина, 1950 г.р. Карцинома мочи-мочевого пузыря с 2009 года, ранее лечилась химиорастворами местно. Уровень Нагаласе на презентации 4 июля 2011 года: 3.10. 10 февраля 2012: 2.30. 25 мая 2012: 1.80. 26 октября 2012: 1.40. Лечение с помощью GcMAF и иглоукалывания, позже только GcMAF (позже внутривенно). Мочевой пузырь признан урологом чистым летом 2012 года. Лечение GcMAF продолжилось.
При этом последовательное снижение активности нагалазы в сыворотке крови ассоциировалось со значительным клиническим улучшением. Снижение активности нагалазы было очевидно при первом тестировании после лечения, примерно через 7 месяцев после начала лечения GcMAF, и сохранялось до последнего доступного определения, т.е. примерно через 15 месяцев после этого. Разница в сывороточной активности нагалазы, зарегистрированная до окончательного определения и до начала терапии GcMAF, составила -1,70 нМоль/мин/мг.
- Женщина, 1944 г.р. Карцинома мочевого пузыря лечится с 2011 года урологом с помощью кюретажа и БЦЖ. Уровень Нагаласе на презентации 9 мая 2011 года: 4.10. 24 октября 2011: 2.30. 3 апреля 2012: 1.40. 10 сентября 2012: 1.00. 4 декабря 2012: 0,75. В период тестирования нагалазы пациенту было рекомендовано еженедельно вводить внутримышечно GcMAF, но пациент не был последовательным. В этот период лечащий уролог несколько раз оценивал состояние мочевого пузыря как хороший. Также в этом случае последовательное снижение активности нагалазы в сыворотке крови ассоциировалось со значительным клиническим улучшением. Такое снижение активности нагалазы было очевидно при первом тестировании после лечения, примерно через 5 месяцев после начала лечения GcMAF, и сохранялось до последнего доступного определения, т.е. примерно через 19 месяцев после этого. Разница в сывороточной активности нагалазы, зарегистрированная до последнего определения и до начала терапии GcMAF, составила -3,35 нМоль/мин/мг. Последнее доступное значение активности нагалазы в сыворотке крови, 0,75 нМ/мин/мг, находилось в пределах нормы.
- Мужчина, 1937 г.р. Карцинома предстательной железы обнаружена с помощью ПСА в 2009 году, специфических жалоб нет. Лечилась гормональными уколами, которые давали жалобы. До и в том же году была обнаружена карцинома толстой кишки, которая была прооперирована после облучения и химиотерапии (нелеченая опухоль/метастазы вероятны). Уровень Нагаласе на презентации 6 апреля 2011 года: 2.00. 29 августа 2011: 1.20. 5 января 2012: 0,81. 5 июля 2012: 0,67. 6 декабря 2012: 0.75. Лечение иглоукалыванием и GcMAF; Через некоторое время гормональное лечение было прекращено, и жалобы, также неспецифические, значительно улучшились. Находится на низкочастотном наблюдении.Активность нагалазы в сыворотке крови вернулась к нормальным значениям (0,75 нМ/мин/мг) примерно через 20 мес лечения GcMAF. Снижение активности нагалазы, однако, было очевидно уже при первом испытании, т.е. через 4 месяца после начала лечения GcMAF. По данным литературы,7 Нормализация уровня нагалазы в сыворотке крови у больных раком предстательной железы может свидетельствовать об эрадикации опухоли.
- Мужчина, 1948 г.р. карцинома предстательной железы в 2008 году; Предстательная железа удалена в 2009 году с хорошим прогнозом. Тем не менее, некоторые сообщения о том, что усталость и боль остались. Было начато лечение GcMAF вместе с несколькими процедурами иглоукалывания. Уровень Нагаласе на презентации 21 октября 2011 года: 1.90. 2 февраля 2012: 1.70. 19 октября 2012: 1.20. Жалобы постепенно уменьшались, и в дальнейшем инъекции стали делать внутривенно. Лечение продолжается.
- Женщина, 1947 г.р. Карцинома левой молочной железы (обнаружена при обследовании), оперирована со сторожевыми узлами в 2010 году, химиотерапия 4 из 6 серий, специфических жалоб не осталось. По-прежнему наблюдается недомогание, усталость и нарушение сна. Уровень Нагаласе на презентации 9 августа 2011 года: 1.70. 16 января 2012: 1.00. 12 марта 2012: 0.72. 11 декабря 2012: 0.60. GcMAF-лечение (преимущественно внутривенное введение) в сочетании с иглоукалыванием. Выпуск GcMAF был прекращен в апреле 2012 года. Количество жалоб уменьшилось. Пациент по-прежнему осматривается раз в несколько месяцев.Значительное снижение активности нагалазы в сыворотке крови наблюдалось после 5 мес лечения GcMAF. Такое снижение сохранялось даже после прерывания GcMAF, а активность нагалазы сыворотки крови нормализовалась примерно через 16 мес после начала терапии. По данным литературы,5 Нормализация активности нагалазы в сыворотке крови у больных карциномой молочной железы может представлять собой показатель эрадикации опухоли.
- Женщина, 1950 г.р. Карцинома левой молочной железы, возможны специфические жалобы, возможны метастазы. После локальной операции облучения грудной клетки в сочетании с химиотерапией, герцептин-терапией. Частично жалобы связаны с лечением. Уровень Нагаласе на презентации 11 мая 2011 года: 5.60. 6 октября 2011: 2.90. 21 февраля 2012: 1.80. 18 октября 2012: 1.10. Лечится внутримышечно, позже внутривенно GcMAF и несколькими процедурами иглоукалывания. Жалоб больше не было (прошло через 3–6 недель), по-прежнему в режиме внутривенного введения GcMAF.Значительное снижение активности нагалазы в сыворотке крови можно было наблюдать примерно через 5 мес после начала терапии. Примерно через 17 мес лечения GcMAF уровень нагалазы в сыворотке крови приблизился к нормальным значениям.
- Мужчина, 1941 г.р. В 2010 году была обнаружена и вылечена карцинома гортани с помощью выскабливания и облучения. Геморрагический ректоколит в анамнезе, жалоб после 2005 года было немного. Карцинома мочевого пузыря обнаружена в 2011 году, лечится местным кюретажем и несколькими циклами БЦЖ-инстилляций. Жалобы, связанные с ростом опухоли и лечением, отсутствие химиотерапии. Лечение состояло из иглоукалывания и внутримышечных инъекций GcMAF, а затем внутривенных инъекций на еженедельной основе. Уровень Нагаласе на презентации 16 мая 2011 года: 4.70. 4 октября 2011: 2.00. 10 февраля 2012: 1.20. 15 июня 2012: 1.00. 23 октября 2012: 0,88. 20 декабря 2012: 0.90. Во время иммунотерапии GcMAF произошли интересные события. Настаивая на экстирпации мочевого пузыря урологами, справился с одной сменой уролога, двумя вторыми мнениями специализированной онкологической клиники, а затем урологом назначенной операционной бригады. Со стороны пациентов было несколько благоприятных изменений в образе жизни, таких как отказ от курения и ежедневное потребление рыбьего жира и листьев шалфея (его собственная инициатива). Несмотря на мнение урологов, я решил давать GcMAF два раза в неделю в течение шести недель. Последним мнением лечащего уролога было отложить окончательное решение до февраля, в связи с гораздо лучшим впечатлением слизистой оболочки мочевого пузыря, начиная с января 2013 года. В сложившейся ситуации у трех названных акторов есть оптимизм.В этом случае значительное снижение сывороточной активации нагалазы после введения GcMAF было связано со значительными клиническими преимуществами, что согласуется с предыдущими отчетами.7
Описательное описание некоторых известных клинических случаев из Соединенных Штатов Америки
Следующие отчеты были переданы ОРЖ и относятся к 2012–2013 годам. У большинства пациентов еженедельный прием 100 нг GcMAF внутримышечно был начат в августе 2012 г., а первая оценка активности сывороточной нагалазы была проведена непосредственно перед началом лечения.
Ни один из пациентов не принимал обычную противоопухолевую химиотерапию во время приема GcMAF. Здесь мы сообщаем только о тех случаях, для которых имелось по крайней мере два определения нагалазы.
- Мужчина, 64 года. Карцинома мочевого пузыря. Уровень Нагалаза при первом тестировании в октябре 2012 года: 2,90. В январе 2013 года: 2,60. Улучшенный.В этом случае снижение активности нагалазы в сыворотке крови могло быть зарегистрировано примерно через 3 месяца лечения GcMAF и ассоциировалось с клиническим улучшением.
- Женщина, 60 лет. Карцинома яичников. Уровень Нагалазы при первом тестировании в июне 2012 года: 3.30. Ноябрь 2012: 2.80. Онкомаркер СА-125 в декабре 2012 г.: 15,7. В феврале 2013 г.: улучшено 19.1.Еженедельное введение GcMAF приводило к значительному снижению активности нагалазы сыворотки крови примерно через 3 мес. Такое снижение было связано с клиническими преимуществами. Эти изменения, однако, не были (пока) связаны со снижением циркулирующего уровня ракового антигена 125 (CA-125), другого опухолевого маркера.
- Мужчина, 67 лет. Карцинома предстательной железы. Уровень Нагалазы при первом тестировании в августе 2012 года: 3,40. В декабре 2012 года: 2,80. Улучшенный.В этом случае клиническая польза была связана со значительным снижением активности нагалазы в сыворотке крови примерно через 4 месяца после начала терапии GcMAF. Эти результаты согласуются с выводами, представленными выше, а также с ранее описанными случаями.7
- Мужчина, 63 года. Плоскоклеточный рак языка. Уровень Нагалазы при первом тестировании в июле 2012 года: 3.00. В сентябре 2012 года: 1,50. В декабре 2012 года: 1.00. Улучшенный.Опять же, клиническое улучшение было связано со значительным снижением активности нагалазы в сыворотке крови, которая приблизилась к нормальному диапазону примерно через 5 месяцев. Насколько нам известно, это первый случай, когда пациент с плоскоклеточным раком языка получает GcMAF. Также пациент n. Тринадцать (Таблица 1) лечили GcMAF по поводу плоскоклеточного рака языка и показали снижение активности нагалазы сыворотки крови примерно через 3 мес.
- Мужчина, 54 года. Колоректальный рак. Уровень нагалазы при первом тестировании в июле 2012 года: 3,90. В октябре 2012 года: 2.00. Прекращено.В этом случае достоверное снижение активности нагалазы в сыворотке крови может быть зарегистрировано примерно через 3 месяца после начала терапии GcMAF. Нам неизвестны причины, которые привели к прекращению лечения.
- Женщина, 58 лет. Плоскоклеточный рак головы и шеи. Уровень Нагалазы при первом тестировании в июне 2012 года: 2,90. В июле 2012 года: 2,70. В феврале 2013 года: 2.00. Улучшенный.В этом случае минимальное снижение активности нагалазы в сыворотке крови, наблюдаемое после 1 мес введения GcMAF, ассоциировалось с клиническими преимуществами.
- Женщина, 35 лет. Плоскоклеточный рак. Уровень нагалазы при первом тестировании в июне 2012 года: 1,50. В сентябре 2012 года: 1.10. Снят с производстваПри этом снижение активности нагалазы в сыворотке крови наблюдалось через 3 мес терапии GcMAF. Нам неизвестны причины, которые привели к прекращению лечения.
- Женщина, 69 лет. Фолликулярная лимфома. Уровень нагалазы при первом тестировании в июне 2012 года: 1,00. В августе 2012 года: 1,30. В январе 2013 года: 1,20. Улучшенный.В этом случае не было выявлено связи между активностью нагалазы в сыворотке крови, лечением GcMAF и клиническими состояниями.
- Женщина, 66 лет. Лимфома. Уровень Нагалаза при первом тестировании в августе 2012 года: 2,20. В ноябре 2012 года: 1,90. Улучшенный.В данном случае клиническое улучшение ассоциировалось со значительным снижением активности нагалазы в сыворотке крови примерно через 3 мес после начала лечения GcMAF.
Обсуждение
Было показано, что GcMAF ингибирует множество аспектов опухолевой трансформации in vitro в различных моделях опухолей.5—10
Описанные здесь клинические случаи неоднородны и относятся к пациентам с разными типами новообразований и на разных стадиях злокачественного прогрессирования.
Эти случаи включают онкологических больных, у которых эффекты GcMAF ранее не были описаны, например, пациенты с различными типами карциномы головы и шеи (включая опухоли гортани и языка), лимфомой, олигодендроцитомой и карциномой яичников. В некоторых случаях пациенты одновременно страдали от нескольких типов опухолей, как сообщается в описании.
Во многих случаях пациенты получали GcMAF вместе с другими дополнительными методами лечения, такими как иглоукалывание или введение пищевых добавок. Во всех случаях терапия GcMAF была начата на поздних стадиях прогрессирования опухоли, так как традиционные методы лечения, очевидно, были предпочтительны на менее поздних стадиях. Таким образом, большинство описанных здесь случаев подпадают под категорию сострадательного обращения.
На самом деле, большинство этих пациентов проходили традиционную противоопухолевую терапию в предыдущие годы и обращались к лечению GcMAF, когда обычная химио- или лучевая терапия оказалась неэффективной или непереносимой, как описано в отдельных отчетах.
Поскольку это открытый, неконтролируемый, ретроспективный анализ, необходимо проявлять осторожность при установлении причинно-следственной связи между лечением и клиническим исходом. Тем не менее, реакция на GcMAF часто была относительно устойчивой, и некоторые тенденции выделяются.
Тенденции из голландских кейсов
- У всех пациентов активность нагалазы в сыворотке крови была значительно выше нормы, то есть около 0,95 нМ/мин/мг.
- У всех пациентов отмечено достоверное снижение активности нагалазы в сыворотке крови после инъекций GcMAF.
- Во всех случаях активность нагалазы в сыворотке крови была снижена при повторной оценке, и такое снижение сохранялось в следующих определениях.
- В 4 из 7 случаев сывороточная активность нагалазы вернулась к нормальному уровню при последней оценке.
Тенденции из американских кейсов
- У всех пациентов, кроме одного, активность нагалазы в сыворотке крови была значительно выше нормы. Пациент #18 действительно имел активность нагалазы в сыворотке крови, которая была очень близка к норме.
- У большинства пациентов наблюдалось достоверное снижение сывороточной активности нагалазы при введении ГцМАФ. У пациентки #18 такое снижение не было связано с клиническими преимуществами, даже несмотря на то, что ее сывороточная активность нагалазы всегда была низкой.
Это отсутствие строгой обратной зависимости между активностью сывороточной нагалазы и клиническими ответами было недавно замечено в исследовании, описывающем эффекты GcMAF у детей с аутизмом. У большинства этих пациентов действительно наблюдалось снижение активности нагалазы в сыворотке крови, а также значительное улучшение симптомов, но эти два явления не были строго коррелированы друг с другом.18
Существенным моментом, который вытекает из анализа описанных выше случаев, является очевидное отсутствие побочных эффектов, связанных с GcMAF. Этот момент, который ранее был задокументирован у аутичных детей,18 имеет большое значение, когда GcMAF рассматривается для сострадательного лечения пациентов с запущенными или неизлечимыми заболеваниями.
Собственно говоря, во многих странах полное отсутствие побочных эффектов является обязательным условием для гуманного применения веществ, которые еще не были одобрены местными санитарными органами.
Очевидно, что эти предварительные наблюдения требуют длительного периода наблюдения для определения наилучших показаний к гуманному назначению GcMAF. На сегодняшний день GcMAF используется (всегда в качестве сострадательной терапии) с обнадеживающими результатами у пациентов, страдающих практически всеми видами рака и на всех стадиях прогрессирования заболевания.
Тем не менее, заманчиво предположить, что пациенты с определенными типами и/или стадиями злокачественных новообразований могут получить устойчивую клиническую пользу от применения GcMAF. Кроме того, генетический фон пациентов, в частности, с точки зрения полиморфизмов VDR, может влиять на индивидуальную реакцию на GcMAF. На самом деле, недавно мы продемонстрировали, что степень ответа моноцитов человека на GcMAF связана с индивидуальными генотипами VDR.13
Таким образом, можно предположить, что такие полиморфизмы также могут влиять на противоопухолевые эффекты GcMAF. Кроме того, следует иметь в виду, что прогноз пациентов, страдающих всеми видами рака, зависит от их алиментарного и воспалительного статуса, который можно контролировать с помощью прогностического индекса воспалительных заболеваний и питания (PINI).19
Таким образом, шкала PINI может стать частью лабораторных оценок, выполняемых в ходе терапии GcMAF, и вместе с оценкой сывороточной активности нагалазы и полиморфизмов VDR может помочь врачам в мониторинге реакции отдельного пациента на GcMAF и корректировке доз и графиков в процессе лечения, если это необходимо.
Исследования, изучающие влияние полиморфизмов GC на ответ онкологических больных на терапию GcMAF, а также вклад различных вариантов GC в относительное количество «неиндуцируемых», неактивных видов GcMAF20 также будет способствовать определению наиболее правильного подхода к администрированию GcMAF.
Результаты, представленные здесь, согласуются с предыдущими результатами5—7 а также с недавней публикацией Inui et al.,21 который описал три клинических случая, успешно лечившихся комбинаторными терапевтическими схемами, включая подкожные или внутримышечные инъекции сыворотки крови человека, содержащей GcMAF. В отличие от этого последнего исследования, результаты, представленные здесь, были получены с помощью высокоочищенного GcMAF, исключающего влияние других сывороточных белков, которые могли действовать как искажающие факторы.
В заключение, представленные клинические случаи подтверждают гипотезу о том, что GcMAF может стать частью противоопухолевых иммунотерапевтических схем.
Материалы и методы
Производство GcMAF
Врачи получили GcMAF от компании Immuno Biotech Ltd (Гернси, Великобритания). GcMAF подвергался высокой степени очистки в соответствии с ранее описанными процедурами.7
Вкратце, VDBP был выделен из очищенной сыворотки крови человека, полученной от Американского Красного Креста, с помощью высокоаффинной хроматографии 25-гидроксивитамина D3-сефарозы или актин-агарозной аффинной хроматографии.
Связанный материал элюировали и далее обрабатывали инкубацией с тремя иммобилизованными ферментами. Полученный GcMAF был стерилизован фильтром.
Содержание белка и концентрацию раствора GcMAF определяли с помощью стандартных методов анализа белка Брэдфорда.22 В конце производственного процесса GcMAF был проверен на стерильность как внутри компании, так и за ее пределами, независимыми лабораториями.
Безопасность и биологическая активность GcMAF были проверены на моноцитах человека,13 клетки рака молочной железы человека,10 и хорионаллантоисные мембраны куриного эмбриона.12
Сбор данных
Ретроспективный обзор карт для анализа тестирования на нагалазу был проведен на первоначальной когорте пациентов, наблюдавшихся клиницистами (RE и д-р Стивен Хофман, CMC, Capelle aan den Ijssel; Нидерланды).
Все записи были просмотрены врачами для подтверждения значений активности нагалазы в сыворотке крови, диагнозов, временных интервалов между тестированием, дозирования GcMAF и клинических ответов. Диагноз рака подтвердили и другие лечащие врачи.
Администрирование GcMAF
Введение GcMAF отдельным пациентам осуществлялось исключительно их лечащими врачами (RE и д-р Стивен Хофман, CMC, Capelle aan den Ijssel; Нидерланды), в соответствии с национальными нормами и правилами.
Оригиналы клинических записей хранятся врачами в соответствующих местах в соответствии с указаниями. В разделе «Результаты» излагаются клинические случаи, максимально приближенные к оригинальным записям врачей, с минимальными грамматическими и орфографическими исправлениями.
Поскольку каждый врач, участвовавший в исследовании, описывал состояние отдельных пациентов по-разному, следует ожидать некоторой неоднородности в этих записях. Примечания специально представлены в том виде, в котором они были написаны, чтобы каждый читатель мог сделать свои выводы.
Определение активности нагалазы в сыворотке крови
Тестирование на нагалазу сыворотки крови проводилось в лабораториях ELN (Банник, Нидерланды) по методике, опубликованной Yamamoto et al.14 В частности, сывороточную активность нагалазы определяли с помощью конечного ферментативного анализа на основе хромогенного субстрата.
Лаборатории ELN установили референсный диапазон 0,32–0,95 нМ/мин/мг субстрата на основе образцов сыворотки, собранных у здоровых добровольцев, что немного выше, чем сообщалось ранее, которое составляло 0,35–0,65 нМ/мин/мг.14 Дальнейшие исследования на повышенном числе испытуемых позволят установить наиболее подходящий референтный диапазон.
Независимо от этого вопроса, поскольку все определения проводились в одной и той же лаборатории, в качестве показателя терапевтической эффективности использовали относительное снижение активности нагалазы в сыворотке крови после введения GcMAF.
Статистические методы
Статистические сравнения между активностью нагалазы в сыворотке крови, наблюдаемой до и после (в двух различных временных точках) введения GcMAF, проводили с помощью t-критерия Стьюдента.
Подтверждения
Авторы выражают благодарность д-ру Стивену Хофману (Steven Hofman), CMC, Capelle aan den Ijssel, Нидерланды, за предоставление данных о пациентах, которых он лечил, а также за критический обзор этого исследования.
Раскрытие информации о потенциальных конфликтах интересов
DN является генеральным директором Immuno Biotech Ltd (компания, занимающаяся выделением и очисткой белка GcMAF). Тем не менее, DN не располагала информацией ни об используемых методах лечения, ни об именах пациентов, чьи данные были проанализированы. Ни он, ни кто-либо из сотрудников Immuno Biotech Ltd не знали ни о нагалазе, ни о результатах других тестов, ни об именах пациентов, использованных в этом исследовании.
Глоссарий
Сокращения:
| Abbreviations: | |
| BCG | bacillus Calmette-Guérin |
| CA-125 | cancer antigen 125 |
| GalNAc | N-acetylgalactosamine |
| GcMAF | GC protein-derived macrophage-activating factor |
| PINI | prognostic inflammatory and nutritional index |
| PSA | prostate-specific antigen |
| VDBP | vitamin D-binding protein |
Сноски
Предыдущая публикация в Интернете: www.landesbioscience.com/journals/oncoimmunology/article/25769
Ссылки
- Ямамото Н., Нарапараджу В.Р., Мур М., Брент Л.Х. Дегликозилирование сывороточного витамин-D3-связывающего белка альфа-N-ацетилгалактозаминидазой, выявленное в плазме крови пациентов с системной красной волчанкой. Клин Иммунол Иммунопатол. 1997; 82:290–8. DOI: 10.1006/clin.1996.4320. [PubMed] [Перекрестная ссылка] [Google Академия]
- Мохамад С.Б., Нагасава Х., Уто Ю., Хори Х. Активность опухолевых клеток альфа-N-ацетилгалактозаминидазы и ее участие в активации макрофагов, связанных с GcMAF. Comp Biochem Physiol A Mol Integr Physiol. 2002; 132:1–8. DOI: 10.1016/S1095-6433(01)00522-0.[PubMed] [Перекрестная ссылка] [Google Академия]
- Греко М., Митри М.Д., Кириако Ф., Лео Г., Бриенца Э., Маффия М. Сывороточный протеомный профиль злокачественной меланомы кожи и связь с прогрессированием рака: связь с активностью альфа-N-ацетилгалактозаминидазы, обусловленной опухолью. Рак Летт. 2009; 283:222–9. DOI: 10.1016/j.canlet.2009.04.001. [PubMed] [Перекрестная ссылка] [Google Академия]
- Редди А.Л., Шанкаранараянан К., Арулрадж Х.С., Деварадж Н., Деварадж Х. Сывороточная альфа-N-ацетилгалактозаминидаза связана с диагностикой/прогнозом пациенток с плоскоклеточным раком шейки матки. Рак Летт. 2000; 158:61–4. DOI: 10.1016/S0304-3835(00)00502-4. [PubMed] [Перекрестная ссылка] [Google Академия]
- Ямамото Н., Суяма Х., Ямамото Н., Ушиджима Н. Иммунотерапия пациентов с метастатическим раком молочной железы витамин-D-связывающим белком-фактором активации макрофагов (GcMAF) Int J Cancer. 2008; 122:461–7. DOI: 10.1002/ijc.23107. [PubMed] [Перекрестная ссылка] [Google Академия]
- Ямамото Н., Суяма Х., Наказато Х., Ямамото Н., Кога Ю. Иммунотерапия метастатического колоректального рака макрофаг-активирующим фактором, полученным из витамина D, GcMAF. Рак Иммунол Иммунотер. 2008; 57:1007–16. DOI: 10.1007/s00262-007-0431-z. [PubMed] [Перекрестная ссылка] [Google Академия]
- Ямамото Н., Суяма Х., Ямамото Н. Иммунотерапия рака предстательной железы фактором, активирующим макрофаги, полученным из белка Gc, GcMAF. Transl Oncol. 2008; 1:65–72. [Бесплатная статья о PMC] [PubMed] [Google Scholar]
- Нонака К., Онидзука С., Исибаси Х., Уто Ю., Хори Х., Накаяма Т. и др. Фактор активации белка и макрофагов витамина D ингибирует ГЦК у мышей с ТКИН. J Surg Res. 2012; 172:116–22. DOI: 10.1016/j.jss.2010.07.057. [PubMed] [Перекрестная ссылка] [Google Академия]
- Грегори К.Дж., Чжао Б., Биленберг Д.Р., Дриди С., Ву Дж., Цзян В., и др. Фактор активации белка и макрофагов витамина D непосредственно ингибирует пролиферацию, миграцию и экспрессию uPAR клеток рака предстательной железы. PLoS One. 2010; 5:Э13428. DOI: 10.1371/journal.pone.0013428. [Бесплатная статья о PMC] [PubMed] [CrossRef] [Google Scholar]
- Пачини С., Пунци Т., Моруччи Г., Гулизано М., Руджеро М. Влияние фактора, активирующего макрофаги, на клетки рака молочной железы человека. Противоопухолевый Res. 2012; 32:45–52. [PubMed] [Google Академия]
- Калкунте С., Брард Л., Гранай К.О., Свами Н. Ингибирование ангиогенеза витамин-D-связывающим белком: характеристика антиэндотелиальной активности DBP-maf. Ангиогенез. 2005; 8:349–60. DOI: 10.1007/s10456-005-9024-7. [PubMed] [Перекрестная ссылка] [Google Академия]
- Пачини С., Моруччи Г., Пунци Т., Гулизано М., Руджеро М. Макрофаг-активирующий фактор (GcMAF) на основе белка Gc стимулирует образование цАМФ в мононуклеарных клетках человека и ингибирует ангиогенез в анализе хорионаллантоической мембраны эмбриона цыпленка. Рак Иммунол Иммунотер. 2011; 60:479–85. DOI: 10.1007/s00262-010-0953-7. [PubMed] [Перекрестная ссылка] [Google Академия]
- Пачини С., Моруччи Г., Пунци Т., Гулисано М., Руджеро М., Амато М. и др. Влияние парикальцитола и GcMAF на ангиогенез и пролиферацию и передачу сигналов мононуклеарных клеток периферической крови человека. Дж.2012; 25:577–81. DOI: 10.5301/jn.5000035. [PubMed] [Перекрестная ссылка] [Google Академия]
- Ямамото Н., Нарапараджу В.Р., Ураде М. Прогностическая ценность сывороточного альфа-N-ацетилгалактозаминидазы и иммуносупрессии в результате дегликозилирования сывороточного белка Gc у больных раком полости рта. Cancer Res. 1997; 57:295–9. [PubMed] [Google Академия]
- Ямамото Н., Линдсей Д.Д., Нарапараджу В.Р., Айрленд Р.А., Попофф С.Н. Дефект в каскаде активации макрофагов, вызванного воспалением, у остеопетротических крыс. Дж Иммунол. 1994; 152:5100–7. [PubMed] [Google Академия]
- Нанн Р. Простой анекдот: доказательства и истории в медицине. J Eval Clin Pract. 2011; 17:920–6. DOI: 10.1111/j.1365-2753.2011.01727.x. [PubMed] [Перекрестная ссылка] [Google Академия]
- Ямамото Н., Ушиджима Н., Кога Ю. Иммунотерапия ВИЧ-инфицированных пациентов фактором активации макрофагов на основе белка Gc (GcMAF) J Med Virol. 2009; 81:16–26. DOI: 10.1002/jmv.21376. [PubMed] [Перекрестная ссылка] [Google Академия]
- Брэдстрит Дж.Дж., Фогелаар Э., Тайер Л. Первоначальные наблюдения повышенной активности альфа-N-ацетилгалактозаминидазы, связанной с аутизмом, и наблюдаемого снижения от инъекций белка-макрофага GC. Аналитика аутизма. 2012; 4:31–8. doi: 10.4137/AUI. С10485. [Перекрестная ссылка] [Google Академия]
- Фабрис А., Бьяджони., Пунци Т., Моруччи Г., Гулизано М., Пачини С. и др. Роль полиморфизмов генов ангиотензинпревращающего фермента и рецептора витамина D в синдроме раковой анорексии-кахексии. Ам Джей Иммунол. 2012; 8:65–70. [Google Академия]
- Редер Д.С., Нельсон Р.В., Борхес К.Р. Статус гликозилирования белка, связывающего витамин D, у онкологических больных. Протеин наук. 2009; 18:2036–42. DOI: 10.1002/pro.214. [Бесплатная статья о PMC] [PubMed] [CrossRef] [Google Scholar]
- Инуи Т., Кучике Д., Кубо К., Метте М., Уто Ю., Хори Х. и др. Клинический опыт интегративной иммунотерапии рака с помощью GcMAF. Противоопухолевый Res. 2013; 33:2917–9. [PubMed] [Google Академия]
- Брэдфорд М.М. Быстрый и чувствительный метод количественного определения микрограммовых количеств белка, использующий принцип связывания белка с красителем. Анальный биохим. 1976; 72:248–54. DOI: 10.1016/0003-2697(76)90527-3. [PubMed] [Перекрестная ссылка] [Google Академия]
